中国医院协会《临床微生物实验室检验质量与安全管理 第1-1部分:通用标准 标准化框架与体系表》团体标准分册公示
ICS 11.020
C 07
团体标准
T/CHAS 10-2-XX―20XX
|
临床微生物检验质量与安全管理
第1-1部分: 总则 标准框架与体系表
Clinical microbiological testing quality and safety management
―― Part 1-1: General principles――Standard framework and system diagram
|
20XX- XX - XX发布 20XX - XX - XX实施
目 次
前言 V
前 言
《临床微生物检验质量与安全管理》团体标准分为以下部分:
――第1部分 总则
――第2部分 基本要求
――第3部分 检验服务
――第4部分 过程管理
――第5部分 技术管理
《临床微生物检验质量与安全管理 第1部分 总则》包括以下部分:
――第1-1部分 总则 标准框架与体系表
――第1-2部分 总则 标准化工作指南
本文件是第1-1部分。
本文件按照 GB/T 1.1-2020规则起草。
本文件由中国医院协会提出并归口。
本文件起草单位:中国科学技术大学附属第一医院(安徽省立医院),中国医学科学院北京协和医院,北京医院 国家卫生健康委临床检验中心,中国药师协会 全国细菌耐药监测网,甘肃省人民医院 甘肃省临床检验中心,上海市东方医院(同济大学附属东方医院),复旦大学附属华山医院抗生素研究所,中国人民解放军总医院,。
本文件主要起草人:马筱玲,杨启文,胡继红,罗燕萍,魏莲花,吴文娟,王明贵、刘月辉、刘晓妤,常文娇,李懿
《临床微生物检验质量与安全管理》
第1-1部分 总则 标准框架与体系表
1 范围
本文件规定了《临床微生物检验质量与安全管理》团体标准的框架和体系表。
本文件适用于指导《临床微生物检验质量与安全管理》团体标准框架内各分册的编制。
下列文件对于本文件的应用是必不可少的。其中,注日期的引用文件,仅该日期对应的版本适用于本文件。不注日期的引用文件,其最新版本(包括所有的修改单)适用于本文件。
GB/T 22576.6 医学实验室质量和能力的要求 第6部分:临床微生物学检验领域的要求
WS/T 442实验室生物安全指南
WS/T 805 临床微生物检验基本技术标准
CNAS-CL02-A001 医学实验室质量和能力认可准则的应用要求
下列术语和定义适用于本文件。
临床微生物检验 clinical microbiological testing
使用符合预期用途的检验技术对临床标本进行检测,以发现、鉴定微生物,评估微生物的致病性和药物敏感性,为感染性疾病的诊断、治疗和预防控制提供科学依据。
3.2
标准体系表 standards system table
按照团体标准各分册的内在联系所形成的明细表,以表示标准体系的结构、层次和各分册要素。
4.1遵循国家相关政策文件,结合国家标准、行业标准和管理规范,构建临床微生物检验质量与安全管理标准体系,对临床微生物检验质量和安全问题进行规范。
4.2 规定临床微生物检验质量与安全管理关键要素,为团体标准内各分册的编制提供指导。
5 标准框架
5.1 按GB/T 13016、GB/T22576.6和 CNAS-CL02-A001设计《临床微生物检验质量与安全管理》团体标准框架,包括总则、基本要求、检验服务、过程管理、技术管理5部分,33项标准。框架见图1。
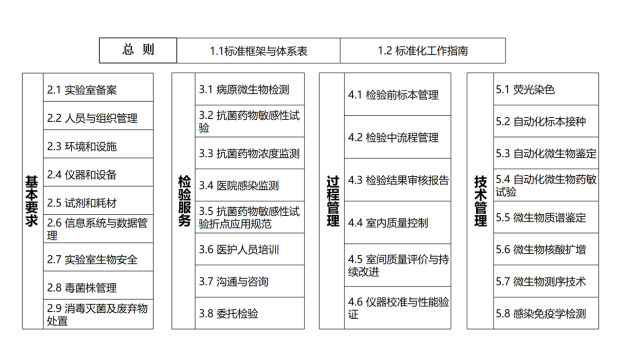
图1《临床微生物检验质量与安全管理》团体标准框架
5.1.1 总则:明确《临床微生物检验质量与安全管理》团体标准的框架、体系表、基本原则、组织与职责、编制要求、工作程序、实施应用、修订更新等要素,用于指导团体标准内各分册的编制,包括:标准框架与体系表、标准化工作指南2个分册。
5.1.2 基本要求:依据GB/T 22576.6、WS/T 442、WS/T 805和CNAS-CL02-A001标准规定,明确临床微生物实验室设置和管理基本要求,包括:实验室备案、人员与组织管理、环境和设施、仪器和设备、试剂和耗材、信息系统和数据安全、实验室生物安全、菌毒株管理、消毒灭菌及废弃物处置等 9个分册。
5.1.3 检验服务:根据医疗机构感染性疾病诊疗需求和GB/T 22576.6、CNAS-CL02-A001标准, 结合《遏制微生物耐药国家行动计划》的目标和任务,明确临床微生物实验室应开展的检验服务内容和质量要求,包括:病原微生物检测、抗菌药物敏感性试验、抗菌药物浓度监测、医院感染监测、抗菌药物敏感性试验折点应用规范、医护人员培训、沟通与咨询、委托检验等8个分册。
5.1.4 过程管理:针对临床微生物检验过程中存在的质量安全风险,依据GB/T 22576.6和CNAS-CL02-A001的要求,设定过程管理内容,包括:检验前标本管理、检验中流程管理、检验结果审核报告、室内质量控制、室间质量评价与持续改进、仪器校准与性能验证等6个分册。
5.1.5 技术管理:针对临床微生物检验技术在使用过程中的质量安全问题,根据风险评估,规范质量与安全管理要求,包括:荧光染色、自动化标本接种、自动化微生物鉴定、自动化微生物药敏试验、微生物质谱鉴定、微生物核酸扩增、微生物测序和感染免疫学检测等8个分册。
6 标准体系表
6.1 根据《临床微生物检验质量与安全管理》团体标准框架,明确各分册的主要内容,具体见表1。
表1 中国医院协会《临床微生物检验质量与安全管理》团体标准体系表
序号 | 编码 | 名称 | 说明 |
第1部分 通用标准 | |||
1 | 1.1 | 标准框架与体系表 | 明确《临床微生物检验质量与安全管理》团体标准编制的指导思想、标准框架和体系表。用于指导团体标准内各分册文件的编制。 |
2 | 1.2 | 标准化工作指南 | 明确《临床微生物检验质量与安全管理》团体标准编制的基本原则、组织与职责、编制要求、工作程序、实施应用和修订更新等要求。用于指导团体标准内各分册文件的编制、应用和修订。 |
第2部分 基本要求 | |||
3 | 2.1 | 实验室备案 | 明确临床微生物实验室在新建和变更时进行备案的基本条件、备案流程以及实验室监管保障等要素。 |
4 | 2.2 | 人员与组织管理 | 明确不同等级医疗机构临床微生物实验室人员配备、组织管理、人员资质、岗位培训和能力考核等要素 |
5 | 2.3 | 环境和设施 | 明确临床微生物实验室环境设计、功能布局和设施配备等要素。 |
6 | 2.4 | 仪器和设备 | 明确不同等级医疗机构临床微生物实验室仪器和设备的配置、使用维护和流程管理等要素。 |
7 | 2.5 | 试剂和耗材 | 明确临床微生物实验室使用试剂和耗材的遴选与采购、 验收与储存、使用与管理等要素。 |
8 | 2.6 | 信息系统与数据管理 | 明确临床微生物实验室信息系统的硬件和软件配置、过程管理、信息和数据安全、持续改进等要素。 |
9 | 2.7 | 实验室生物安全 | 明确临床微生物实验室生物安全管理要求、操作技术规范和安全保障等要素。 |
10 | 2.8 | 菌毒株管理 | 明确临床微生物实验室菌毒株管理原则、管理制度、菌毒株保藏资质、保存方法、使用管理和安全管理等要素。 |
11 | 2.9 | 消毒灭菌及废弃物处置 | 明确临床微生物实验室不同环境和物品消毒灭菌方法、废弃物处置规定及风险评估和改进的基本要求。 |
第3部分 检验服务 | |||
12 | 3.1 | 病原微生物检测 | 明确不同等级医疗机构病原微生物检测能力、检测技术管理、质量评价和持续改进的基本要求。 |
13 | 3.2 | 抗菌药物敏感性试验 | 明确不同等级医疗机构抗菌药物敏感性试验检测能力、检测技术管理、质量评价和持续改进的基本要求。 |
14 | 3.3 | 抗菌药物浓度监测 | 明确临床微生物实验室开展抗菌药物浓度监测的试验条件、监测方法、质量管理与评价改进的基本要求。 |
15 | 3.4 | 医院感染监测 | 明确临床微生物实验室在医院感染监测中的职责任务、监测技术、质量管理与评价改进的基本要求。 |
16 | 3.5 | 抗菌药物敏感性试验折点应用规范 | 明确临床微生物实验室进行抗菌药物敏感性试验时折点的选择原则、规范性应用、评价与改进的基本要求。 |
17 | 3.6 | 医护人员培训 | 明确临床微生物检验人员对本医疗机构内医护人员进行培训的目标任务、培训过程、效果评价与持续改进的基本要求。 |
18 | 3.7 | 沟通与咨询 | 明确临床微生物检验人员为保证检验质量和检验结果合理应用与医护人员、患者及家属进行沟通与咨询的方式、内容、过程管理、效果评价与持续改进的基本要求。 |
19 | 3.8 | 委托检验 | 明确临床微生物实验室需进行委托检验时,委托项目的备案、受委托实验室选择、委托检验过程和质量管理的基本要求。 |
第4部分 过程管理 | |||
20 | 4.1 | 检验前标本管理 | 规范临床微生物检验前标本采集、运输、接收和验收的技术要求、过程管理、质量评价和持续改进等关键要素。 |
21 | 4.2 | 检验中流程管理 | 规范临床微生物实验室检验中微生物培养鉴定和抗菌药物敏感性试验的技术要求、过程管理、质量评价和持续改进等关键要素。 |
22 | 4.3 | 检验结果审核报告 | 规范临床微生物检验结果审核、报告及质量改进等各要素。 |
23 | 4.4 | 室内质量控制 | 规范临床微生物实验室主要仪器、试剂和检测方法室内质量控制的基本要求、质控方案、质控标准及失控处理等关键要素。 |
24 | 4.5 | 室间质量评价与持续改进 | 规范临床微生物检验能力评价方法、质量指标、检验结果互认和质量持续改进等关键要素。 |
25 | 4.6 | 仪器校准与性能验证 | 规范临床微生物实验室仪器校准与性能验证的方法和质量标准。 |
第5部分 技术管理 | |||
26 | 5.1 | 荧光染色 | 规范荧光染色技术在感染病原体鉴定中的应用范围、技术管理及质量管理要求。 |
27 | 5.2 | 自动化标本接种 | 规范自动化标本接种系统的技术管理、性能验证及质量管理要求。 |
28 | 5.3 | 自动化微生物鉴定 | 规范自动化微生物鉴定仪使用的基本条件、技术管理及质量管理要求。 |
29 | 5.4 | 自动化微生物药敏试验 | 规范自动化药敏系统应用的基本条件、技术管理及质量管理要求。 |
30 | 5.5 | 微生物质谱鉴定 | 规范微生物质谱鉴定技术使用的通用要求、技术管理及质量管理要求。 |
31 | 5.6 | 微生物核酸扩增 | 规范微生物核酸扩增检测技术应用的基本要求、技术管理及质量管理要求。 |
32 | 5.7 | 微生物测序技术 | 规范微生物测序技术应用的基本要求、技术管理及质量管理要求。 |
33 | 5.8 | 感染免疫学检测 | 规范感染免疫学检测技术的应用范围、技术管理及质量管理要求。 |
[1] 国家卫生健康委员会,等.遏制微生物耐药国家行动计划(2022-2025年)[Z].国卫医函〔2022〕185号,2022-10-25.
[2] GB/T 22576.6 医学实验室质量和能力的要求 第6部分:临床微生物学检验领域的要求
[3] WS/T 805 临床微生物检验基本技术标准
[4] WS/T 442 实验室生物安全指南
[5] CNAS-CL02-A001 医学实验室质量和能力认可准则的应用要求
[6] 马筱玲,胡继红,徐英春,等.临床微生物学实验室建设基本要求专家共识[J].中华检验医学杂志,2016,39(11):820-823.
[7] 杨启文,倪语星,林丽开,等.临床微生物实验室真菌检测能力建设基本要求专家共识[J].中华检验医学杂志,2019,42(7):514-528.
[8] 王辉,马筱玲,钱渊,等.临床微生物学手册(第12版)[M].北京:中华医学电子音像出版社, 2020.
[9] 尚红,王毓三,申子瑜.全国临床检验操作规程[M].第4版.北京:人民卫生出版社,2015.
[10] 丛玉隆,马筱玲,尹一兵,等.实用检验医学下册(第 3 版)[M].北京:人民卫生出版社,2025.




